Simulación de proteínas oncogénicas por Dinámica Molecular y diseño de fármacos in silico
14/01/2025
Zheyao Hu, estudiante becado por China Scholarship Council, defendió su tesis doctoral Titulada “In silico design of inhibidores de RAS oncogenic proteínos y estrategias para blocking de tumour growth” y dirigida por el dr. Jordi Martí Rabassa el 14 de enero de 2025 en el Campus Nord de la UPC. La tesis presenta un estudio detallado del comportamiento de los oncogenes de la familia RAS, relacionados con un tercio del total de cánceres que existen, y propone una nueva metodología para lograr el diseño por ordenador de fármacos capaces de bloquear la activación de los oncogenes. Como ejemplo, se proponen dos prototipos de fármacos, uno de ellos potencialmente adecuado para tratar a pacientes con cáncer de páncreas y otro para pacientes con melanoma
Esta Tesis Doctoral está dedicada al estudio de las propiedades estructurales de los oncogenes RAS, que tienen una influencia fundamental en el 30% de los tumores humanos, principalmente cánceres de páncreas, pulmón, colon y piel. Las proteínas RAS son una familia de importantes reguladores moleculares que desempeñan un papel clave en una amplia variedad de funciones celulares como la proliferación, diferenciación, adhesión o apoptosis. Estas proteínas son interruptores binarios entre guanosina-difosfatasa (GDP) y guanosina-trifosfatasa, pudiendo regular las redes de señalización citoplasmática, esenciales en el crecimiento, diferenciación y supervivencia de las células.
Desde el punto de vista técnico, se han aplicado simulaciones de dinámica molecular clásica (en una escala de 10 microsegundos) y simulaciones de metadinámica bien temperada (WTM), de modo que todos los sistemas considerados han sido modelados a nivel totalmente atómico, con sistemas de hasta a 250000 átomos. La aplicación de simulaciones WTM de 1 microsegundo, ha permitido realizar por primera vez cálculos de energía libre relacionados con la unión de diversas sondas moleculares con modelos de membranas celulares en solución acuosa. Las superficies de energía libre investigadas muestran un comportamiento específico de los enlaces de moléculas pequeñas, como la benzotiadiazina, en las membranas de fosfolípidos.
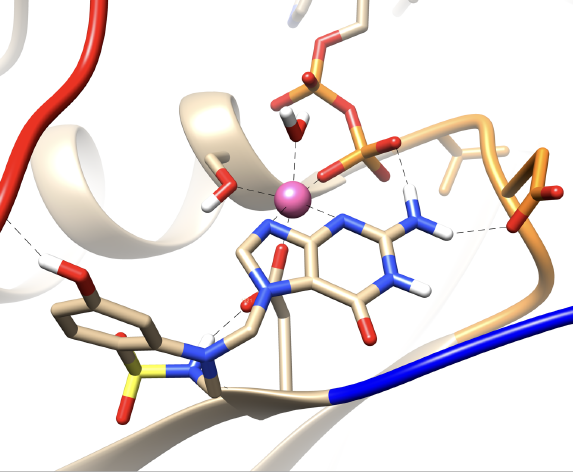
Aunque las mutaciones de KRAS-G12D son uno de los impulsores oncogénicos más frecuentes en los cánceres humanos, todavía no se ha aprobado clínicamente ningún agente terapéutico dirigido directamente a KRAS-G12D, por lo que sigue estando libre de fármacos. Hemos descubierto que el cofactor Mg2+ juega un papel crucial en los cambios conformacionales del complejo KRAS-GDP, hemos localizado dos novedosos bolsillos dinámicos farmacológicos exclusivos de KRAS-G12D y hemos diseñado in silico el inhibidor DBD15-21-22, que puede apuntar -se específicamente y de cerca al complejo ternario KRAS-G12D-GDP-Mg2+ proporcionando una estrategia adecuada para su inhibición. También se ha propuesto otro inhibidor (HM-387) para tratar tumores relacionados con el oncogén NRAS-Q61R.
Compartir: